[환경미디어= 김한결 기자] 식품의약품안전처(처장 김강립)는 액상 고분자, 세라믹 분말 등의 신소재를 이용한 환자 맞춤형 3D 프린팅 치과용 의료기기를 위한 허가‧심사 가이드라인 2건을 발간했다.
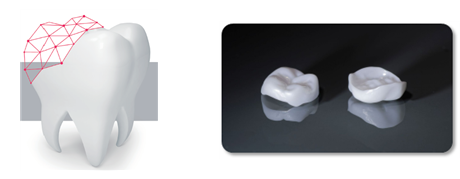 |
| ▲ 3D 프린팅으로 제작된 제품 외형(크라운 등 치아의 일부 또는 전체를 대체하는 치과보철물을 만드는 재료로 세라믹 분말로 제작) <제공=식품의약품안전처> |
주요 내용은 ▲허가‧인증‧신고 절차 및 항목 ▲3D 프린팅 제조공정을 고려한 적층기술 등 기재사항 ▲안전성‧유효성 입증자료 요건 ▲성능평가 항목 및 시험방법 등이다.
3D 프린팅 기술로 제작된 치과용 의료기기를 사용하는 경우 의료진의 정밀하고 정확한 시술을 가능하게 하고 시술시간을 단축시킬 수 있고, 특히 환자에게는 시술 후 불편함을 줄일 수 있다.
이에 따라 치과용 의료기기 관련 분야에서 3D 프린팅 기술이 활발하게 활용되고 있다.
식약처 관계자는 “4차 산업혁명 시대의 변화하는 환경에 발맞추어 새로운 기술에 대한 허가‧심사방안을 선제적 마련하고, 혁신적인 의료기기의 제품화를 적극 지원해 나겠다”고 밝혔다.
이번 가이드라인은 식약처 홈페이지에서 확인할 수 있다.
[저작권자ⓒ 이미디어. 무단전재-재배포 금지]











































